علاجات واعدة لفقر الدم المنجلي
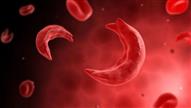
فقر الدم المنجلي
د ب أ-
قال الدكتور ربيع حنّا، أخصائي أمراض الدم وأورام الأطفال في مستشفى كليفلاند كلينك للأطفال، إن التعامل مع مرض فقر الدم المنجلي يشهد حاليا تطورات لافتة ومثيرة، لا سّيما مع التقدم، الذي تم تحقيقه في مجال الأبحاث وتطوير علاجات جديدة من شأنها منح ملايين المرضى حول العالم أملا حقيقيا بالتعافي.
وأضاف حنّا أن مرض فقر الدم المنجلي يمكن أن يؤثر بشدة على جودة حياة المرضى ويحد من إمكاناتهم بسبب نوبات الألم الشديدة وتلف الأعضاء الطرفية وانخفاض متوسط العمر المتوقع؛ حيث يمكن للأدوية تخفيف شدة المرض وعلاج الأعراض، التي يسببها، ولكن متوسط عمر المريض يكون عادةً في منتصف الأربعينيات، ولهذا من المهم للغاية الوصول إلى علاج فعّال لهذا المرض.
تغير جيني في الحمض النووي
ويتسبب التغير الجيني في الحمض النووي لدى الأشخاص المصابين بهذا المرض في حدوث تغير كيميائي في الهيموجلوبين - وهو بروتين أحمر مسؤول عن نقل الأكسجين في الدم - ما يؤدي إلى تحوّل الخلايا إلى ما يشبه شكل "المنجل" بدلا من شكلها الطبيعي المستدير، الأمر الذي يعيق مرورها بسهولة عبر الأوعية الدموية، كما يمكنها أيضا أن تسدَّ الأوعية أو تتفكك، ما يؤدي إلى انخفاض عمر خلايا الدم الحمراء وزيادة معدل تخزين الحديد في الكبد والقلب.
ويمكن أن يؤدي ذلك إلى إصابة المريض بمضاعفات خطيرة مثل تليف الكبد وفشل الكبد والسكتة الدماغية واعتلال عضلة القلب وفشل القلب هذا بالإضافة إلى الآلام الشديدة.
زراعة الدم أو النخاع
وتشمل الخيارات العلاجية للمصابين بهذا المرض عمليات زراعة الدم أو النخاع، ولكن في الواقع من الصعب العثور على متبرع متطابق كما أن هناك مخاطر كبيرة مرتبطة بهذا النوع من العلاجات.
وأوضح الدكتور حنّا هذه المخاطر قائلاً: "أولا، تتراوح نسبة مخاطر عدم تقبل جسم المريض للخلايا الممنوحة بين 5٪ و 10٪. ثانيا، هناك خطر الإصابة بمرض "الطعم حيال المضيف"graft-versus-host disease ، والذي يحدث عندما يهاجم نخاع عظم المتبرع أو الخلايا الجذعية المتلقي. ولتفادي مثل هذه الحالة، يتم إعطاء المريض أدوية قوية مثبطة للمناعة، ولكن لا يزال هناك خطر كبير للإصابة بمرض الطعم حيال المضيف".
علاج جيني
وأضاف الدكتور حنّا: "في المقابل يعتمد العلاج الجيني على الخلايا الجذعية الخاصة بالمريض، وبالتالي، يتم التخلص من مخاطر عدم تقبل المريض للخلايا أو احتمالية الإصابة بمرض الطعم حيال المضيف".
ومن الفوائد الأخرى للعلاج الجيني أن المرضى لن يحتاجوا إلى أدوية مثبطة للمناعة؛ لذا سيعمل جهاز المناعة لديهم بشكل طبيعي، وهو أمر مهم بشكل خاص خلال الجائحة. بالإضافة إلى ذلك، بينما يحتاج المرضى إلى العلاج الكيميائي لتعزيز جهوزية الجسم سواءً عند إجراء عمليات زراعة تقليدية أو عمليات العلاج الجيني، فإن العلاج الكيميائي المستخدم في العلاج الجيني يكون أقل قوة.
وتابع الدكتور حنّا: "يمثل العلاج الجيني تقنية رائدة تعمل عن طريق استبدال أو تعطيل الجينات المسببة للأمراض. ونقوم في تجربتنا السريرية التي نجريها حالياً بإدخال جينات صحية وسليمة في الجسم بهدف تصحيح التشوهات الجينية لخلايا الدم الحمراء. ومن خلال تمكين الخلايا من إنتاج المزيد من الهيموجلوبين الجنيني، فإن هذا العلاج لديه القدرة على علاج مرض فقر الدم المنجلي بطريقة دقيقة".
أدوية جديدة
ومن الأدوية، التي تمت الموافقة عليها من جانب إدارة الغذاء والدواء الأمريكية (FDA) خلال عامي 2019 و2021 على التوالي، دواء crizanlizumab ، والذي يعمل على تقليل الآلام والمضاعفات الشديدة، ودواءvoxelotor ، والذي يساعد على استعادة الوظائف الطبيعية لخلايا الدم الحمراء وتوصيل الأكسجين إلى الأنسجة، مما يساعد بالتالي على تخفيف الألم.
ووفقا لبيانات منظمة الصحة العالمية، فإن نحو 5٪ من سكان العالم يحملون جينات السمات المسببة لاضطرابات الهيموجلوبين، وخاصة مرض فقر الدم المنجلي والثلاسيميا. ومع ذلك تجدر الإشارة إلى أن هذا لا يعني أنهم سيصابون بالمرض. وتشير التقديرات إلى أن 300000 طفل يولدون سنويا مع اضطرابات شديدة في الهيموجلوبين. وتعتبر الهند وبعض بلدان الشرق الأوسط وأفريقيا من بين تلك، التي ينتشر فيها مرض فقر الدم المنجلي.
فيديو قد يعجبك: